【先発医薬品販売会社による自社特許権に関する情報提供や謹告の業界紙への掲載行為は、後発品販売承認を希望する会社に対する不競法上の信用毀損行為に該当しないとされた事例】
投稿日:2026年4月22日 |

著者:弁理士 佐藤 眞紀
|
参照条文/キーワード/論点 |
不正競争防止法(不競法)2条1項21号/他人の営業上の信用を害する虚偽の事実/医薬品/後発品承認 |
ポイント
※ 本件は、先発医薬品イグザレルト®を製造販売するバイエル社が、自社特許権に関する情報提供を厚生労働省に行ったり、謹告を業界紙に掲載したりする行為が、後発品承認申請を実施していた日本ジェネリック株式会社(JG)に対する不競法上の信用毀損行為に該当するかが争われた事案である。 |
判決概要 |
| 裁判所 | 東京地方裁判所第46部 |
| 判決言渡日 | 令和7年10月29日 |
| 事件番号 | 令和7年(ワ)第70139号 |
| 事件名 | 不正競争防止法違反に基づく差止等請求事件事件 |
| 裁判長裁判官
裁判官 裁判官 |
高橋 綾
西山 芳樹 瀧澤 惟子 |
事案の概要
1.バイエル主張の特許権
・JP4143294(物質特許:リバーロキサバンそのものをクレーム)
・JP4852423(製法、製剤のクレーム)
・JP5147703(非結晶形化に関する製法等をクレーム、年金不払いにより放棄)
・JP5311742(製法)
・JP5416408(結晶型をピークで特定、年金不払いにより放棄)
2.事件の時系列
・2008/6/20 JP4143294登録。
・2012/1/18 イグザレルト®承認取得。
・2020/1/17 イグザレルト®再審査期間満了。
・2020/12/4~2024/7/29 バイエルは日刊薬業に6回、謹告を掲載。
・2023/2月 JGが、リバーロキサバンOD錠について製造販売申請。
成人SPAFとVTEの2つのIndicationで申請。
審査過程で、MHLWの照会に応じてバイエルは特許の見解(「回答」)を提出した。
・2024/8/15 JGは、効能効果SPAF(用途2)のみのMA取得。
・2025/3/26 JGは、効能効果VTE(用途1)の効能追加申請実施。
・2025/10/29 判決言渡
3.JP4143294の延長登録状況
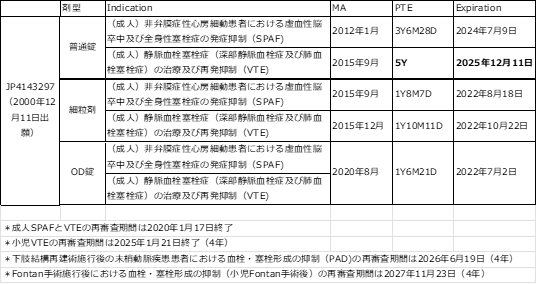
争点
争点1:本件謹告の掲載が、「他人の営業上の信用を害する虚偽の事実」の流布に当たるか
争点2:本件回答が「他人の営業上の信用を害する虚偽の事実」の告知に当たるか
争点3:「営業上の利益を侵害されるおそれ」の有無
争点4:「故意または過失により不正競争を行って他人の営業上の信用を害した」に当たるか
争点5:正当な行為として違法性が阻却されるか
裁判所では、争点1および2について検討された。
争点に関する当事者の主張
(1)争点1
(原告の主張)
ア 本件謹告は、「原告製品が本件発明の延長登録後の権利範囲に含まれるとの見解」を示したものであるから、「他人の営業上の信用を害する」(不競法2条1項21号)ものといえる。
本件謹告に原告製品を特定する記載はないが、①本件特許権を含む3件の特許権について、延長登録を取得済み又は出願中であり、
これらの特許権及び延長登録は有効であると共に実効性があるものと確信していること、
リバーロキサバンを有効成分とする製品の製造、販売、輸入等を計画されている企業は、
被告の知的財産権の侵害行為のなきよう十分留意してほしいこと等が記載されているから、
リバーロキサバンを有効成分とする後発医薬品の製造販売行為は
被告の保有する特許権を侵害するとの事実を含意している
といえること、②令和2年12月4日から令和6年7月29日までの間に合計6回
も掲載されていること、③本件回答では、後発医薬品として原告製品が特定されている
ことに照らせば、厚労省等は本件謹告が原告製品を対象にする(少なくとも、原告製品を対象に含む)ものと当然に理解する。
イ 特許権侵害の存否に関する見解も
「事実」(不競法2条1項21号)に当たる。そして、以下のとおり、
普通錠についての延長登録(本件延長登録3及び4)後の本件特許権の効力は、
OD錠である原告製品には及ばず、
その製造販売は本件特許権の侵害に当たらないから、本件謹告は「虚偽」(同号)に当たる。
(ア) オキサリプラティヌム大合議判決は、医薬品として政令処分対象物と実質同一なものに存続期間が延長された特許権の効力が及ぶとした上で、医薬品の有効成分のみを特徴とするいわゆる物質特許については、「有効成分ではない「成分」に関して、対象製品が、政令処分申請時における周知・慣用技術に基づき、一部において異なる成分を付加、転換等しているような場合」(以下「第一類型」という。)のみを実質同一なものに含まれる類型として挙げているところ、同判決の判示等に照らせば、物質特許について実質同一と認められるのは第一類型に限られると解すべきである。
本件特許は物質特許であるところ、本件延長登録3及び4に係る政令処分対象物(普通錠)と原告製品(OD錠)の有効成分は同一であるものの、添加剤の成分が大きく異なり、しかも、原告が本件延長登録3及び4に係る政令処分の申請後に相違する成分やその含有量に関する2件の特許権(特許第7511596号、特許第7641098号)を取得していることからすると、第一類型に当たるものとはいえない。
(イ) 本件特許について、OD錠についての本件延長登録9及び10の存続期間は既に満了しており、上記OD錠はパブリックドメインになったということができるから、普通錠についての延長登録(本件延長登録3及び4)後の権利範囲に上記OD錠を含めることは、特許権者と第三者の衡平を欠き、延長登録制度の趣旨に反する。
(被告の主張)
ア 本件謹告は、文面上、リバーロキサバンを有効成分とする製品の製造、販売、輸入等を計画している企業に対し、被告の保有する知的財産権の侵害があると認める場合には相応の手段を講じるという被告の姿勢を表明したものにすぎず、具体的な後発医薬品に係る特許権侵害の事実に言及したものではない。
したがって、本件謹告は、特定の他人(原告)の財産上の義務履行について受ける社会的信頼を害するものではなく、「他人の営業上の信用を害する」ものとはいえない。
イ 前記アのとおり、本件謹告は、知的財産権侵害に対する被告の姿勢を表明したものにすぎず、「事実」ではない。
また、仮に本件謹告が、原告製品の製造販売が延長登録後の本件特許権の権利範囲に含まれることを示すものであるとしても、以下のとおり、本件用途1に係る普通錠についての延長登録(本件延長登録3及び4)後の本件特許権の効力は、効能又は効果に本件用途1を含む原告製品に及ぶから、本件謹告は「虚偽」ではない。
●(省略)●
(2)争点2
(原告の主張)
ア 被告は、厚労省に本件回答をし、厚労省はPMDAに情報提供をしたから、被告は、本件回答により、厚労省のみならずPMDAに対しても告知をしたものといえる。
イ 本件回答は、原告製品について製造販売の承認申請をしている原告の営業上の信用を害するものであるから、「他人の営業上の信用を害する」(不競法2条1項21号)ものといえる。
ウ 特許権侵害の存否に関する見解も「事実」(不競法2条1項21号)に当たるところ、前記⑴(原告の主張)イと同様に、本件回答は「虚偽」(同号)に当たる。
(被告の主張)
ア 厚労省からPMDAに情報提供があったことは不知。
イ 本件回答は、医薬品の承認審査の過程における厚労省の照会に対する回答であって、その他の様々な情報と共に行政機関である厚生労働大臣の判断の参考にされるにとどまり、その内容も、先発医薬品メーカーとして抽象的な法的見解を表明したものにすぎないから、原告の財産上の義務履行について受ける社会的信頼を害するものとはいえず、「他人の営業上の信用を害する」ものとはいえない。
ウ 本件回答は、特許権の権利範囲に関する法的見解を表明したものにすぎないから、「事実」ではない。
この点を措いても、前記⑴(被告の主張)イと同様に、本件回答は「虚偽」ではない。
判旨
<争点1>本件謹告の掲載が、「他人の営業上の信用を害する虚偽の事実」の流布に当たるか
⑴・・・しかしながら、前記前提事実⑷のとおり、本件謹告は、要旨、①被告は、リバーロキサバンを有効成分とする製品を保護する特許として、本件特許権を含む5件の特許権を保有し、本件特許権を含む3件については、それぞれの製品の承認に基づき延長登録を取得済み又は出願中であって、
そして、業界紙に掲載された本件謹告の読者は同業者を含む製薬業の関係者であると認められるところ、本件延長登録によって本件特許権の存続期間(当初は令和2年12月11日)が延長されたことからすると、上記のような内容の本件謹告を業界紙に掲載することで同業者に対する情報提供や注意喚起を図ることは、先発医薬品メーカーとして、後発医薬品の製造販売等による特許権侵害を防止する上で自然な対応であったと考えられる。
以上によれば、読者の普通の注意と読み方とを基準にした場合に、本件謹告は、リバーロキサバンを有効成分とする後発医薬品の製造販売行為について、剤型や用途等を含むその構成によっては、先発医薬品についての本件特許権を侵害することがあり得るという当然の事項を前提に、被告がリバーロキサバンに係る特許権を侵害する行為等には権利を行使する方針であることを一般的に述べることによって、情報提供ないし注意喚起したものと理解するというべきであり、原告製品を含む特定の後発医薬品との関係での本件特許権の権利範囲についての見解を示すものと理解するとは考え難い。
以上によれば、本件謹告が、「他人の営業上の信用を害する」(不競法2条1項21号)ものであるとはいえない。
したがって、本件謹告の掲載は、同号所定の不正競争に当たらない。
⑵ これに対し、原告は、①本件謹告はリバーロキサバンを有効成分とする後発医薬品の製造販売行為が被告の保有する特許権を侵害するとの事実を含意しているといえること、②令和2年12月4日から令和6年7月29日までの間に合計6回も掲載されていること、③本件回答では、後発医薬品として原告製品が特定されていることに照らせば、厚労省等は本件謹告が原告製品を対象にする(少なくとも、原告製品を対象に含む)ものと当然に理解すると主張する。
しかしながら、上記①②について、本件謹告が、リバーロキサバンを有効成分とする後発医薬品の製造販売行為が先発医薬品についての本件特許権を侵害することがあり得るという当然の事項を前提に権利行使の方針を述べたものと理解できるのは前記⑴に説示したとおりであり、本件謹告から理解される内容は、その掲載回数の多寡や掲載期間の長短によって、変わるものではない。
また、上記③について、厚労省等が、本件回答により、被告において、●(省略)●との見解を有している(前記前提事実⑹)ことを認識したとしても、本件謹告から理解される内容が前記⑴のとおりのものであることに変わりはない。そうすると、厚労省等が、本件謹告について、原告製品を含む特定の後発医薬品との関係での本件特許権の権利範囲についての見解を示すものと理解するとは認められない。
したがって、原告の主張を採用することはできない。
<争点2>本件回答が「他人の営業上の信用を害する虚偽の事実」の告知に当たるか
⑴ 不競法2条1項21号は、「競争関係にある他人の営業上の信用を害する虚偽の事実を告知し、又は流布する行為」が不正競争に当たる旨規定している。
そして、
⑵ 医薬品の製造販売の承認は、厚生労働大臣が、医薬品等の品質、有効性及び安全性の確保並びにこれらの使用による保健衛生上の危害の発生及び拡大の防止のために必要な規制として、薬機法により与えられた権限と責任に基づいてする行政処分であって、自由競争が行われる取引社会における取引とは性質が異なる。そして、厚労省等が、後発医薬品の承認審査に当たり、先発医薬品と後発医薬品との特許抵触の有無を確認するため、必要に応じて、先発医薬品の特許権者等に補足説明を求めることは、行政処分に先立つ情報収集行為であって、そこでは、厚労省等において、後発医薬品の申請者の経済的価値に対する社会的評価を形成することが想定されているとはうかがわれない。また、厚生労働大臣は、後発医薬品の承認審査において、先発医薬品の特許権者等からの提供情報だけでなく、諸般の事情を総合考慮し、自らの権限と責任においてその判断をするものである上に、先発医薬品の特許権者等から提供される情報は一般に公開しないとされている(前記前提事実⑹ア)のであるから、同情報が市場に伝ぱして取引社会における申請者の経済的価値に関する社会的評価が低下するおそれがあるということもできない。
⑶ 以上によると、被告が、厚労省による原告製品の承認審査の過程で、先発医薬品の特許権者等として説明を求められたのに対し、●(省略)●との見解を有している旨の回答(本件回答)をして情報提供することは、「他人の営業上の信用を害する」(不競法2条1項21号)ものであるとはいえない。
したがって、本件回答は、不競法2条1項21号所定の不正競争に当たらない
解説/検討
第二条 この法律において「不正競争」とは、次に掲げるものをいう。
…(略)…
二十一 競争関係にある他人の営業上の信用を害する虚偽の事実を告知し、又は流布する行為
後発品会社は、承認前に特許権侵害否認判断を得るルートが閉ざされている(ニプロv. エーザイ「ハラヴェン事件」[知財高裁令和4(ネ)10093号])。そこで、後発会社が非侵害(無効)と確信する特許の情報を、先発会社がMHLWに提出するというパテントリンケージ対応は不競法上の信用毀損行為に該当するか?という形でサムソン・バイオエピスのアイリーアのケースおよび本件は争った。
結局本件では、サムソンv. リジェネロンの知財高裁判決を踏襲する形で、特許権者が審査過程で行う情報提供は「取引社会における社会的評価を低下させるものではない」とし不競法上の信用毀損行為は否定された。特許権の有効性や侵害性は検討されておらず、今後も不競法上の信用毀損が認められるハードルは高そうである。
ところで、原告が特許権非侵害を主張する理由であった「普通錠について延長された特許権(PTE)の効力が、OD錠に及ぶか」についての判断は回避された。PTEの効力範囲は製薬会社にとっては重要な論点であるが、未だ不透明な点が多い。この点について、最近では用量が異なる錠剤に関する東京地裁の判決があり(ルビプロストンカプセルに関する判決、令和7年(ワ)第10786、10790号、特許権侵害差止請求事件、2026年3月3日判決言渡)、更なる判決の積み重ねが期待される。