【添付文書改訂は特許権存続期間延長登録の理由となる処分に該当しないとされた事例】
投稿日:2026年5月8日 |

著者:弁理士 池田 直俊
|
参照条文/キーワード/論点 |
特許法67条4項/特許法施行令2条2号イ/添付文書改訂/処分/延長登録出願 |
ポイント知財高裁は、添付文書は製造販売承認の対象ではなく、PMDAの助言も行政指導に留まるため、添付文書改訂は特許権存続期間延長登録の理由となる処分には当たらないと判断した。 |
判決概要 |
| 裁判所 | 知的財産高等裁判所第3部 |
| 判決言渡日 | 令和7年5月26日 |
| 事件番号 | 令和6年(行コ)第10007号 |
| 事件名 | 延長登録出願却下決定取消請求控訴事件 |
| 裁判長裁判官
裁判官 裁判官 |
中平 鍵
今井 弘晃 水野 正則 |
事案の概要
本件は、製造販売承認済み医薬品「ガザイバ®点滴静注1000mg」について、添付文書改訂の情報がPMDA(医薬品医療機器総合機構)のウェブサイトに掲載された日を「処分を受けた日」として延長登録出願をしたところ、特許庁長官がこれを却下したため、控訴人(ロシュ)がその取消しを求めた事案である。
控訴人は、添付文書の改訂は実質的に一部変更承認と同等であり、特許法施行令2条2号イの類推適用がされるべきであるものであると主張した。
しかし知的財産高等裁判所は、添付文書改訂は医薬品医療機器等法(以下、薬機法)上の「承認」に当たらないと判断し、原判決(請求棄却)を支持した。
この判決は、医薬品の「添付文書改訂」や行政指導に基づく事実を延長理由として主張する延長登録出願は基本的に拒絶されることを示すものといえる。
1.背景
(1)本件特許発明1
【請求項1】
オビヌツズマブを含有するCD20陽性のB細胞性リンパ腫治療用医薬組成物であって、前記医薬組成物は、1回の投与あたりオビヌツズマブとして1000mgが点滴静注され、2回以上のサイクルにおいて、以下の(a)及び(b):
(a)初回サイクルの投与におけるオビヌツズマブの最大投与速度が、200mg/時以上、好ましくは300mg/時以上、より好ましくは400mg/時以上、
(b)2回目以降のサイクルの投与における開始投与速度が、オビヌツズマブ100mg/時、最大投与速度が、オビヌツズマブ800mg/時以上、
の投与速度に従い投与される医薬組成物
(2)承認、特許登録、添付文書改訂の経過
2018年7月2日 本件承認日
2018年7月 改定前添付文書がPMDAウェブサイトに掲載された日
2018年8月29日 薬価基準収載日
2020年8月4日 添付文書改訂のための臨床試験開始
2021年3月30日 本件特許の登録日
2021年10月 PMDAへの添付文書改訂の相談
2021年12月9日 改定後添付文書がPMDAウェブサイトに掲載された日(「処分を受けた日」として主張)
(3)添付文書(2024年6月改定(第4版))

(4)「使用上の注意」等の改訂について(2021年11月2日)

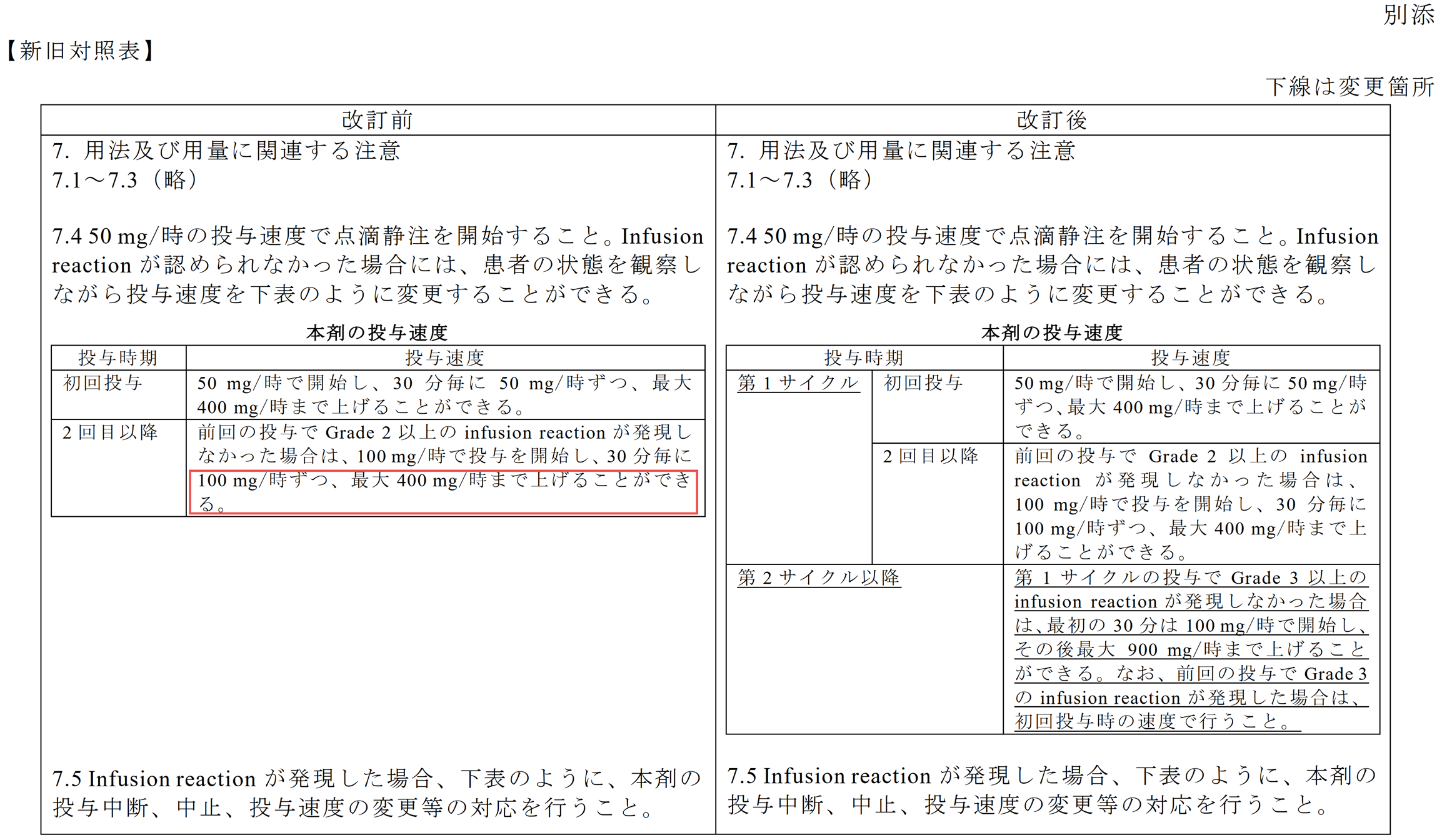
本件承認時点の添付文書には、投与速度を「最大400mg/時まで上げることができる」と記載されていたが、添付文書の用法・用量に関する使用上の注意の記載が改訂され、「最大900mg/時まで上げることができる」と、投与速度の上限が拡張された。
(5)延長登録出願
控訴人(ロシュ)は、添付文書改訂の情報がPMDAのウェブサイトに掲載された日を「処分を受けた日」として延長登録出願をしたところ、特許庁長官がこれを却下したため、その取消しを求めて訴えた。
争点に関する当事者の主張
2.控訴人の主張
2-1.控訴の趣旨
特許庁長官がした令和5年3月14日付け手続却下処分を取り消す。
2-2.控訴人の具体的主張
本件医薬品の投与速度に関する添付文書改訂は、手続的には製造販売承認における一部変更承認と同等であり、特許法施行令2条2号イの類推適用がされるべきであるものである。
(1)一部変更承認と本件届出等とは実質的に同じである
・製造販売承認時に、用法・用量とこれに関連する使用上の注意は一体として審査・指示され、その際に最大投与速度の上限が設定された。
・本件届出は、用法・用量に関連する使用上の注意に記載された最大投与速度の上限を引き上げるために行われた。
・一部変更承認(改正前薬機法14条9項)と本件届出はいずれも、(i)臨床試験の成績を手続資料として提出する必要がある、(ii)薬事当局による有効性及び安全性の審査を受ける必要がある、(iii)使用態様(投与速度など)の許容範囲が拡張される、という点で一致している。
・添付文書改訂相談では、PMDAがその了承に反した届出を不受理にする権限を持ち、相談を経ない届出や助言に従わない届出は実質的に排除されており、PMDAの了承が事実上不可欠である。
(2)規制権限を有する当局からの「助言」は強制性を有する
・規制権限を行使し得る立場の者から、その権限を行使され得る立場の者に対して助言が行われる場合、単なる行政指導を超えて実質的な権限行使としての側面を持つ。
・PMDAは助言に従わない届出を不受理にできる権限を有する。
・実態としてPMDAは、その了承に反した添付文書改訂の届出を不受理にすることが可能であり、相談を経ない届出や助言に従わない届出は実質的に排除されている。
・直接届出の手続フローが存在せず、助言遵守が必須である。
・PMDAは添付文書改訂相談を経ずに直接届出がされる場合の手続フローを準備しておらず、被控訴人によっても直接届出事案や助言に従わずに届出が受理された例は確認できない。
・PMDAによる届出の受理がなければ改訂後添付文書で医薬品を販売できず、受理により初めて改訂後の添付文書を使用する権利が発生する。
(3)本件届出(添付文書改訂)は、特許法施行令2条2号イ注1の類推適用がされるべきである
・原判決は施行令の「処分」を限定列挙とみて類推適用を否定したが、限定列挙と解する具体的理由を示していない。
・PMDAの指示で「使用上の注意」に上限数値が明示されれば上限超過は実質禁止となり、一部変更承認によって用法・用量に含めた場合と実質同様である。
・製造販売後臨床試験に基づく改訂で上限引上げ(使用態様拡張)を行う手続・効果は一部変更承認と同じである。
・施行令が未整備で、制度の不備を補うため類推適用を認めるべきである。
・本件では特許発明の実施が事実上禁止された期間が存在。
・特許法67条2項の趣旨(実施不能期間の回復)に合致し、実質同様の手続で保護に大差が出るのは制度不備である。
・平成23年最判も延長の目的を「処分を受けるために実施できなかった期間の回復」とするところ、本件にも実施不能期間があるため類推適用が妥当。
注1特許法67条4項において、存続期間を延長できるものは政令(特許法施行令)で定められるものであることが規定されている。そして、特許法施行令2条2号イにおいて、薬機法に係る承認が規定されている。
判旨
当裁判所も、控訴人の請求は理由がないから棄却すべきであると判断した。
(1)棄却理由(判決文抜粋)
・「本件承認は、本件医薬品の投与速度(最大許容投与速度)をそもそも対象としていないのであるから、本件投与方法に係る添付文書の改訂を内容とする本件届出等が、本件承認の一部変更に当たると解する余地はない。」
・「添付文書自体は、製造販売の承認の対象とはされていない。」
・「承認申請時に提出された添付文書は、製造販売の承認の審査時にPMDAにおいて確認を行い、その記載内容について助言等をすることがあるにしても、これは必要に応じ行政指導として行われるものにとどまる。」
・「本件医薬品を本件投与方法に沿って800mg/時以上の投与速度等で投与することは、添付文書の改訂以前においても、本件承認の下において、法令上禁止されていたものということはできず、・・・そのため、本件届出等による添付文書の改訂により、本件投与方法の使用の禁止が解除されたものでないことは明らかである。」
・「特許権の存続期間終了後は何人も自由にその発明を利用できるとするのが特許制度の根幹の一つであるとする平成11年最判の趣旨にも鑑みれば、みだりに同条の規定を拡張又は類推して解釈すべきではない。」
(2)控訴人主張に対する裁判所判断(判決文抜粋)
・「本件承認に関連して、添付文書に係るPMDAの指示は行政指導により行われたものであるから、PMDAの指示により本件医薬品の最大投与速度の上限が定められた事実は存しない。」
・「本件届出等により、実施可能な投与速度の許容範囲が拡張されたものでもないから、控訴人の主張はいずれも前提を欠くものである。」
・「本件届出等が一部変更承認と実質的に同じものとはいえないし、PMDAの指示が強制力を有するものとも認められない。」
・「特許法施行令2条2号に定める「処分」については限定列挙と解されるところであり、その改正の経緯に鑑みても、平成30年の添付文書改訂相談制度の導入以後も控訴人の主張するような改正が行われないことを、直ちに特許法施行令ないし現行制度の不備と捉えるべきものとは解されない。」
解説/検討
本判決は、特許法67条4項に基づく「処分」の解釈について、医薬品の「添付文書改訂」やPMDAによる「助言」が「処分」に該当しないことを判示し、これらは行政指導にとどまるものであることと位置付けた。すなわち「承認」や「一部変更承認」といった法的処分の範囲を厳格に限定する姿勢を示したといえる。
実務的には、製造販売承認後に得られた臨床データに基づき用法・用量の変更や添付文書の改訂が行われても、それがいかに実質的な規制的影響をもたらすとしても、「処分」に該当しない限りは特許権存続期間の延長登録の対象とはならないことが改めて確認されたことになる。