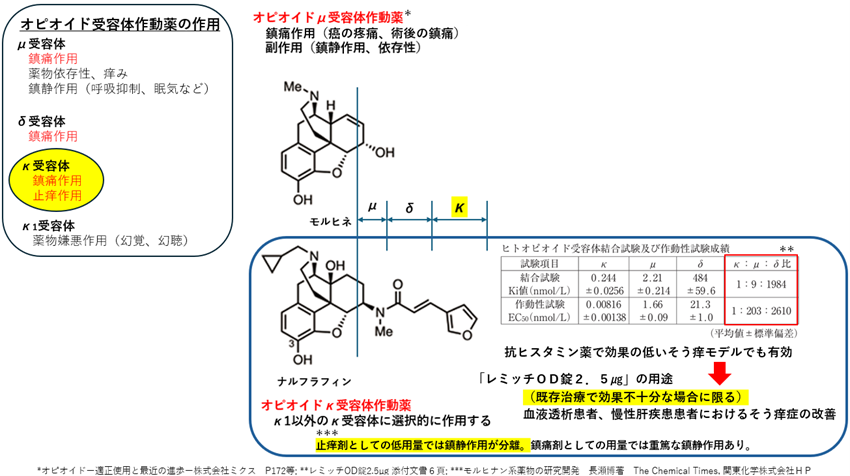
【発明の技術的範囲の属否判断と、存続期間の延長登録がされた特許権の侵害について通常実施権者の損害賠償請求権を認めた事例】
投稿日:2026年5月11日 |

著者:弁理士 大栗 由美
|
参照条文/キーワード/論点 |
特許法102条1項、特許法102条3項、特許法79条、特許法68条の2/有効成分/塩酸塩/フリー体/延長登録/通常実施権者の損害賠償請求権 |
ポイント塩酸塩を有効成分とする被告製剤について、「有効成分」の技術常識に基づき、「化合物を有効成分とする止痒剤」である本件発明の技術的範囲に属すると判断された事案である。また、先行する既承認医薬品である軟カプセル剤の試験期間をOD錠の承認に伴う本件延長登録の期間に算入することは妥当であると判示した。さらに、損害賠償請求権について、民法709条の不法行為は、「法律上保護される利益」が侵害された場合に成立するものであるとして、通常実施権者の損害賠償請求権を認めた。 |
判決概要 |
| 裁判所 | 知的財産高等裁判所第2部 |
| 判決言渡日 | 令和7年5月27日 |
| 事件番号 | 令和3年(ネ)第10037号 |
| 事件名 | 特許権侵害差止等請求控訴事件 |
| 裁判長裁判官
裁判官 裁判官 |
清水 響
菊池 絵理 頼 晋一 |
事案の概要
[対象特許]
特許第3531170号(本件特許)
(出願日平成9年11月21日(優先権主張1996年11月25日))
[延長登録出願]
・出願番号2015-700061
[政令処分の内容]
対象:「ノピコールカプセル2.5㎍」
有効成分「ナルフラフィン塩酸塩」
用途:慢性肝疾患患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
出願日:平成27年3月25日
延長登録日:平成27年7月15日(延長の期間5年)
・出願番号2017-700309
[政令処分の内容]
対象:「レミッチカプセル2.5㎍」
有効成分「ナルフラフィン塩酸塩」
用途:(既存治療で効果不十分な場合に限る)透析患者(血液透析患者を除く)、慢性肝疾患患者におけるそう痒症の改善
出願日:平成29年11月20日
延長登録日:平成30年7月25日(延長の期間5年)
・出願番号2017-700310
[政令処分の内容]
対象:「レミッチOD錠2.5㎍」
有効成分:「ナルフラフィン塩酸塩」
用途:(既存治療で効果不十分な場合に限る)透析患者(血液透析患者を除く)、慢性肝疾患におけるそう痒症の改善
出願日:平成29年11月20日
延長登録日:平成30年7月25日(延長の期間5年))
・出願番号2017-700154
[政令処分の内容]
対象:「レミッチOD錠2.5㎍」
有効成分:「ナルフラフィン塩酸塩」
用途:(既存治療で効果不十分な場合に限る)血液透析患者、慢性肝疾患
患者におけるそう痒症の改善
出願日:平成29年6月29日
延長登録日:令和3年8月11日(延長の期間5年))
[本件特許]
本件特許は発明の名称を「止痒剤」とする「オピオイドκ受容体作動性化合物を有効成分とする止痒剤」に関するものである。
【請求項1】
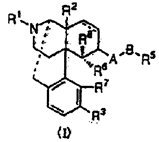
[式中、
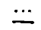
は二重結合又は単結合を表し、R1は炭素数1から5のアルキル、炭素数4から7のシクロアルキルアルキル、炭素数5から7のシクロアルケニルアルキル、・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・を表す。また、一般式(I)は(+)体、(-)体、(±)体を含む]で表されるオピオイドκ受容体作動性化合物を有効成分とする止痒剤。
[本件医薬品]
本件医薬品の成分である塩酸ナルフラフィンは実施例9に記載された下記化合物7に相当する。
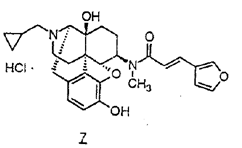
レミッチOD錠2.5μg
本件医薬品は、東レ株式会社が開発し、鳥居薬品(JT子会社)が独占的通常実施権者として販売
争点
<[1]侵害論
(1)被告製剤は本件発明の技術的範囲に属するか(争点1)
(2)被告製剤は本件発明に記載された構成と均等なものか(争点2)
(3)(欠番)
(4)本件延長登録等により存続期間が延長された本件特許権の効力は被告製剤の製造販売等に及ぶか(争点4)
(5)本件延長登録等は、本件発明の実施のために、本件処分等(医薬品「レミッチ OD 錠2.5㎍」に係る承認処分)を受けることが必要であったとは認められない場合であり無効にされるべきことから、原告による本件特許権の行使は権利濫用か(争点5)
(6)本件延長登録等は、延長期間が本件発明の実施をすることができなかった期間を超えており無効にされるべきものか(争点6)
(7)先使用権の存否(争点7)
[2]損害論
(1)特許法102条1項に基づく損害に関する争点
ア 鳥居薬品の損害賠償請求権の成否(争点8)
イ 単位数量当たりの利益の額(争点9)
ウ 販売することができないとする事情の有無及び当該事情に相当する数量
等(争点10)
(2)特許法102条3項等に基づく損害に関する争点
適正な実施料(争点11)
(3)損害一般に関する争点
ア 消費税相当額を加算して損害を算定することの可否(争点12)
イ 原告の損害額(争点13)
争点に関する当事者の主張・判旨
[1]侵害論
(1)被告製剤は本件発明の技術的範囲に属するか(争点1)および(2)被告製剤は本件発明に記載された構成と均等なものか(争点2)
(1)について
<原告>
本件発明の「有効成分」は、・・・・・・薬効を生じる薬理作用を奏する成分であると理解される。そうすると、本件発明における「有効成分」はナルフラフィンと解される。・・・・・・被告製剤は、ナルフラフィンを「有効成分」とする止痒剤であるから、本件発明の構成要件を充足し、その技術的範囲に属する。
<被告>
本件発明は、特許請求の範囲請求項1の解釈上、塩酸塩を除外しているから、その技術的範囲はナルフラフィン(フリー体)に限定され、ナルフラフィン塩酸塩は含まない。出願経過においても、原告はナルフラフィン塩酸塩を意識的に除外している。よって、ナルフラフィン塩酸塩が本件発明の技術的範囲に属すると主張することは信義則違反であるし、本件発明で特定、限定されているナルフラフィン(フリー体)が、延長登録によって酸付加塩に広がることもない。
(2)について
<原告>
・・・・・・本件特許の出願経過を考慮しても、被告製剤(ナルフラフィン塩酸塩を有効成分とする止痒剤)が意識的に除外されたとする特段の事情はない。
<被告>
均等侵害に関し、特許請求の範囲の補正又は訂正による減縮によって対象製品等が含まれないことが明らかになった場合は、第5要件の特段の事情があるというべきところ、本件では、補正前の請求項1では、対象化合物にナルフラフィン(フリー体)とナルフラフィン塩酸塩の双方が含まれているようにも見えていたものが、補正により含まれないことが明らかになったのであるから、特段の事情がある。
✔裁判所の判断
イ 本件明細書の記載(判決文37頁)
・・・・・・そう痒の治療には、内服剤として抗ヒスタミン剤、抗アレルギー剤などが主に用いられ、・・・・・・しかし内服剤の場合、作用発現までに時間のかかることや、中枢神経抑制作用(眠気、倦怠感)、消化器系に対する障害などの副作用が問題となっている。・・・・・・従来よりオピオイド系作動薬は痒みを惹起し、その拮抗薬が止痒剤としての可能性があるとされてきた。しかし、オピオイド系拮抗薬を止痒剤として応用することは現在までのところ実用化されていない。
本発明の目的は、上記の問題点を解決した止痒作用が極めて速くて強いオピオイドκ受容体作動薬およびこれを含んでなる止痒剤を提供することにある。」(12頁12行目~13頁23行目)
ウ「有効成分」に関する文献の記載等(判決文43頁)
❶「医薬品の有効性とは治療効果であり、・・・・・・・製剤より有効成分がどの程度生体内へ利用されているかを測定する必要がある。・・・・・・この生体への医薬品有効成分の利用率をBioavailability と称し、通常は投薬後一定時間おきに血液や尿を採取し、血清中や尿中に存在する(吸収され、代謝をうけ、また排泄された)有効成分の含量の時間的推移をしらべる・・・・・・」(甲79)
❷「「生物学的利用能とは、活性を有する薬物成分あるいは治療有効成分が医薬品製剤から吸収され、薬の作用部位で利用されるようになる速さや量である」とされている。具体的には、有効成分の血中濃度、尿中排泄あるいは薬理効果を測定することが定められているが、・・・・・・」(甲80)
❸「・・・・・・錠剤を内服したとき、胃とか腸とかで崩れて、効きめをもった成分が放出されることが第一段階になる。有効成分が吸収され、血流で体内に広く分布され、一部は血中のタンパク質と結びつき、また脂肪組織などに貯えられるかもしれない・・・・・・」(甲81)
・・・・・・
❷「製剤中に含まれている有効成分は、投与された後に、製剤から放出あるいは溶出される必要があります。・・・・・・それら製剤を投与後の有効成分の血中濃度や作用発現部位中の濃度は推定でき、ヒト試験の代わりになるのではと期待される面があります。」(甲86)
❸「レミッチ錠のようないわゆる低分子医薬品の経口剤においては、錠剤(OD錠)又はカプセルから溶け出した有効成分が消化管(主に小腸)から吸収されて、循環血液中に移行し、薬効を発揮します。循環血液中の有効成分が血流によって全身の組織・器官へ運ばれ、・・・・・・この薬効を発揮する有効成分の体内での存在状態を確認するため、有効成分の血中濃度が測定され、また、有効成分の消化管での溶出挙動を確認するために溶出試験が実施されます。・・・・・・」
「・・・・・・上記の有効成分有効成分を効率よく消化管で吸収させ、薬効を発揮させるために、血中に移行する有効成分に対して・・・・・・」
エ 「塩基性薬物」に関する文献の記載等(判決文47頁) 省略
オ 本件特許の出願経過(判決文48頁)
・平成13年4月24日付けで拒絶理由通知
・原告は、平成13年7月16日付けで意見書及び手続補正書を提出し、・・・・・・本件補正において、原告は、補正前の請求項1~3のうち、拒絶理由通知で指摘を受けた請求項1及び2を削除し、これに伴い、請求項3を請求項1に改めるなどしたが、本件補正の補正後の請求項1においては、補正前の請求項3で引用していた補正前の請求項2の「またはその薬理学的に許容される酸付加塩」の文言が欠落している。

カ 本件発明1の技術的範囲の検討(判決文50頁)
(ア)請求項1には、「κ受容体作動性化合物又はその薬理学的に許容される酸付加塩」を有効成分とする止痒剤との表現は用いられていない。しかし、本件明細書の記載によれば、「オピオイドκ受容体作動薬」は、「オピオイドκ受容体作動性を示すモルヒナン誘導体またはその薬理学的に許容される酸付加塩」であり、・・・・・・等とされている。また、本件明細書の実施例9においても、「選択的なκ受容体作動性オピオイド化合物である…モルヒナン塩酸塩7」と記載されており、化合物とその酸付加塩の形態とは厳密に区別されていない。
(イ)しかるところ、「有効成分」の用語は、前記…のとおり、本件特許出願の日の前後を通じて、体内(血中)で溶出し薬理作用を発揮する化学物質の意味で用いられる場合が一般的に見られていたものであり、本件明細書において、これと異なる解釈をとるべき理由は見当たらない。・・・・・・酸付加塩の形態を含めて「有効成分」と呼ぶ取扱いが存在することは認められるが、付加された塩の部分が体内で薬理作用を発揮する化学物質になるわけではない。
(ウ)もともと、本件発明の目的は、止痒作用が極めて速くて強いオピオイドκ受容体作動薬及びこれを含んでなる止痒剤を提供することにある。製剤の技術分野において、本件特許の出願当時、薬物の溶解性や安定性を向上させるために酸付加塩の形態をとることは、技術常識であったと認められ、本件明細書の記載によっても、酸付加塩の形態について、それ以外の技術的意義があることを認めるに足りない。したがって、本件明細書をみた当業者は、本件発明の目的である止痒作用を発揮する化学物質は「κ受容体作動性化合物」であって、「薬理学的に許容される酸付加塩」の形態は、物質の止痒作用自体を変化させるためのものではなく、薬としての溶解性や安定性を向上させるための形態にすぎないことは容易に理解することができたはずである。・・・・・・当業者において、請求項1に「オピオイドκ受容体作動性化合物を有効成分とする止痒剤」とだけ記載されていることを理由に、その趣旨が、「薬理学的に許容される酸付加塩」は、本件発明1でいう有効成分には当たらず、特許の技術的範囲外であると解釈するとは考えられない。止痒剤に関する特許において、合理的理由もないのに、わざわざ酸付加塩の形態という薬としての溶解性や安定性を向上させるために通常よく用いられる構成を除外して、特許請求の範囲を決めることは不自然だからであり、むしろ、本件明細書の前記各記載によれば、「κ受容体作動性化合物の薬理学的に許容される酸付加塩」の形態は、κ受容体作動性化合物を有効成分とする止痒剤の実施形態の一つであることを容易に理解することができるというべきである。
(エ)前記オの本件特許の出願経過を参酌しても、原告は、本件補正により、補正前の請求項3の一般式(Ⅰ)を含む発明を補正後の請求項1に補正し、その際「またはその薬理学的に許容される酸付加塩」の文言を欠落させたことが認められるが、拒絶理由通知においては、補正前の請求項3は拒絶の対象にされておらず、原告の意見書においても、一般式(Ⅰ)の化合物に対する言及を含め、・・・・・・補正後の請求項1において「またはその薬理学的に許容される酸付加塩」の文言を欠落させたことについての説明はされていない。そうすると、本件特許の出願経過において、原告が、本件補正の際に、補正後の請求項1から「酸付加塩」の文言を意識的に除外したと認めることはできないというべきである。
・・・・・・、特許請求の範囲及び本件明細書の記載、本件特許の出願経過及び本件特許出願日当時の技術常識によれば、本件発明1は、酸付加塩の形態をとるか否かにかかわらず、一般式(Ⅰ)で表される化合物が、生体内において溶出して吸収され、そのオピオイドκ受容体作動性という属性に基づき「有効成分」としての薬理作用を発揮するような止痒剤をいうものと解するのが相当である。
・・・・・・被告製剤は、本件延長登録出願に係る特許権の請求項1に係る本件発明1の技術的範囲に属するものと認めるのが相当である。また、争点2(均等論)については、判断を要しない。
(4)本件延長登録等により存続期間が延長された本件特許権の効力は被告製剤の製造販売等に及ぶか(争点4)
✔裁判所の判断
前記のとおり、被告製剤は本件発明1の技術範囲に属し、その製造販売等は本件発明1の実施に該当するから、問題は、当該実施が対象物についての実施ということができるかどうかである。・・・・・・特許法68条の2の対象物の範囲は、延長登録の制度趣旨及び特許権者と第三者との衡平を考慮し、特許法の観点から合理的に解釈すべきものである。すなわち、存続期間が延長された特許権の効力を、薬機法に基づく処分で定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」についての実施のみに限定したときは、少しでも成分等が異なれば特許権の効力が及ばなくなるから、存続期間延長により特許権者を保護しようとした法の趣旨にそぐわない結果となる。他方、薬機法に基づく処分の対象となった「物」とはおよそ異なる「物」についての実施にも特許権を及ぼすことは、同条の文理に明らかに反することになる。そこで、薬機法に基づく処分で特定された「物」から出発し、特許発明の技術的意義及び政令処分の内容に照らし、これと医薬品として「実質同一」であると認められる範囲の物についての実施に限り、延長後の特許権の効力が及ぶと解するのが相当である。そうすると、本件における対象物には原告製剤と医薬品としての「成分、分量、用法、用量、効能及び効果」が特許法の観点から実質同一であると認められるものも含まれるというべきである。
しかるところ、本件発明1が本件特許出願当時既に公知の物質であった「一般式(Ⅰ)で表されるκ受容体作動性化合物」を止痒剤としての作用効果を有する有効成分として用いた用途発明である点に発明としての技術的特徴があること、後記のとおり、本件処分等は、前記一般式(Ⅰ)で表されるκ受容体作動性化合物のうちナルフラフィンを有効成分とする止痒剤である本件発明1を実施し、前記補正の上引用した原判決の前提事実⑵エの本件処分及び同⑵ウの310号処分の各処分の内容に示される原告製剤であるレミッチOD錠2.5㎍の製造販売をするために必要な処分であったことを踏まえると、原告製剤と被告製剤がナルフラフィンを有効成分とする止痒剤という点でその技術的特徴及び作用効果が同一であり、かつ、医薬品としての具体的な剤形を同一にする場合において、被告製剤が、有効成分ではない「成分」に関して、政令処分申請時における周知・慣用技術に基づき、一部において異なる成分を付加、転換等しているにすぎないと認められるときや、有効成分以外の被告製剤との「成分」等の差異が医薬品としての「効能及び効果」に影響を与えず、当該差異が僅かな差異又は全体的にみて形式的な差異にすぎないと認められるときは、医薬品としては、本件処分の対象となった原告製剤と実質同一なものに該当するというべきである(知財高裁平成28年(ネ)第10046号平成29年1月20日特別部判決参照)。
・・・・・・原告製剤と被告製剤は、いずれも、一般式(Ⅰ)で表されるκ受容体作動性化合物であるナルフラフィンを有効成分とする止痒剤であり、レミッチカプセル2.5㎍との生物学的同等性が確認された医薬品である。両製剤は、いずれも、経口投与剤として、レミッチカプセル2.5㎍と有効性及び安全性において違いの生じないOD錠となるように開発され、また、被告製剤の用途は原告製剤の用途の開発に合わせたものと解されるものであり、その「有効成分、分量」及び「用法、用量、効能、効果」は同じであり(前記(2)ウ)、両製剤は有効成分を除く添加剤の限度で成分を異にするものにすぎない。しかるところ、一般に、添加剤とは、前記技術常識のとおり、その製剤の投与量において薬理作用を示さず、無害であり、また、有効成分の治療効果を妨げないものとして加えられるものである。原告製剤に係る本件明細書等の前記記載や、被告製剤の開発経過に照らしても、両製剤に使用されている各添加剤がこれと異なる技術的意義を持つものとは認められない。
ウ 原告製剤と被告製剤は、・・・・・・その技術的特徴及び作用効果が同一であり、かつ、医薬品としての具体的な剤形も同一である。原告製剤と被告製剤のこれらの共通点や前記の添加剤の意義に照らすと、原告製剤と被告製剤の添加剤における差異は僅かな差異又は全体的にみて形式的な差異に当たり、被告製剤は、医薬品として本件処分等の対象となった原告製剤と実質同一なものに該当するというべきである。
エ したがって、本件延長登録等により存続期間が延長された本件特許権の効力は被告製剤の製造販売等に及ぶものと認めるのが相当である。
(5)本件延長登録等は、本件発明の実施のために、本件処分等(医薬品「レミッチ OD 錠2.5㎍」に係る承認処分)を受けることが必要であったとは認められない場合であり無効にされるべきことから、原告による本件特許権の行使は権利濫用か(争点5)
✔裁判所の判断
ア 原告製剤は、前提事実(2)のとおり、本件処分等の対象となった医薬品であり、販売名を「レミッチOD錠2.5㎍」、有効成分を「ナルフラフィン塩酸塩」とするものである(甲35)。
イ 原告製剤の医薬品製造販売承認書(甲35)の「成分及び分量又は本質」欄には、成分として「ナルフラフィン塩酸塩」が記載されている。また、「規格及び試験方法」欄では、溶出試験において、ナルフラフィンのピーク面積に基づいて、ナルフラフィン塩酸塩の溶出率が算定されている。
・・・・・・
原告製剤は、延長登録出願に係る特許権の請求項1に係る本件発明1の技術的範囲に属するものと認めるのが相当であり、かつ、原告製剤の製造販売等という具体的な実施行為を行うためには、薬機法の定めるところに従い、本件処分等を受ける必要があったことが認められるから、旧特許法67条2項(現4項)の延長登録の要件が満たされていたというべきである。
(6)本件延長登録等は、延長期間が本件発明の実施をすることができなかった期間を超えており無効にされるべきものか(争点6)
<被告>
被告らは、本件延長登録等について、特許発明の実施をすることができなかった期間は、生物学的同等性試験の臨床試験の期間と審査期間を加えた期間の1年11月26日になるから、延長期間はこれを超えているなどと主張する。
・・・・・・被告らは、承認申請が剤形追加の場合には、生物学的同等性試験結果を提出し、これにより有効性及び安全性が確認されており、また、参考資料として先行処分(本件では軟カプセル剤)の臨床試験結果を提出することがあっても、改めて審査されるわけではないから、先行処分の試験期間を「前記政令で定める処分を受けるために特許発明を実施することができなかった期間」に算入することはできず、これを算入すべき特段の事情も存在しないなどと主張する。
✔裁判所の判断
本件では、「剤形追加に係る医薬品」の承認申請時に提出を求められる「生物学的同等性」資料だけでなく、既承認医薬品につき実施された試験に関する記載のある添付文書(案)や、既承認医薬品(レミッチカプセル2.5㎍等)に関する審査報告書等の資料が提出されたことで、前記各臨床試験が、原告製剤の有効性及び安全性を検証し、確認するために必要な評価試料として、各審査で用いられ、その結果、本件処分がされたことが推認される。これらのレミッチカプセルに関する試験等は、本来、当初からカプセル剤ではなく、OD錠の承認を求める場合には、当然に必要とされていたはずのものであるから、本件において、これらの先行処分に係る既承認医薬品の試験期間を算入することが不合理であるということはできない。
<被告>
被告らは、OD錠の承認に伴う本件延長登録等に軟カプセル剤の臨床試験期間を再度算定することは、実質的に二重に臨床試験期間を回復することになり制度趣旨に反するなどと主張する。
✔裁判所の判断
医薬品における「前記政令で定める処分を受けるために特許発明を実施することができなかった期間」は、薬機法に基づく当該医薬品の承認手続の内容、承認による禁止解除の範囲についての解釈を踏まえ、特許法の観点から個別に判断されるものである。本件においては、OD錠である原告製剤を製造販売等するためには、本件処分等により禁止解除を得る必要があったところ、・・・・各試験が「承認を受けるのに必要な試験」であったと認められる・・・・現に軟カプセル剤に関する試験結果や効能・効果の内容等については、OD錠に関する本件処分等の承認申請手続においても資料が提出されて審査対象とされたことが認められる。・・・・・・軟カプセル剤の承認を受けただけで、本件処分等を受けることなくOD錠の剤形で本件特許を実施することができるわけではない。以上によれば、本件延長登録等によって延長された期間が、前記政令で定める処分を受けるために特許発明を実施することができなかった期間を超えるものと認めることはできない(旧特許法125条の2第1項3号)。よって、この点に関する被告らの主張を採用することはできない。
(7)先使用権の存否(争点7)
<被告>
被告沢井製薬においては、原告の本件延長登録出願前にOD錠の独自開発を行って特許出願等を行い、臨床試験等も行い後発医薬品の製造販売承認申請をして承認後に被告製剤を上市しているから、特許法79条を類推適用して先使用権を認めるべきであるなどと主張する。
✔裁判所の判断
被告沢井製薬が上市した被告製剤については、既に公開されている本件特許に基づき、その実施品として製造販売する事業の準備等がされていたのであり、被告沢井製薬は、仮に本件延長登録出願を知らなかったとしても、本件特許の存在及びその内容は公開されていたから、被告沢井製薬において、これを知り、又は容易に知り得たはずである。このような場合にまで通常実施権を認めることは、特許の存続期間の延長制度により特許を実施することができない事情があった特許権者の保護を図る趣旨を損なうことになり、むしろ当事者間の公平に反する結果となる。したがって、本件においては同条を類推適用する前提がないというべきであるから、被告らの主張を採用することはできない。
[2]損害論
(1)特許法102条1項に基づく損害に関する争点
ア 鳥居薬品の損害賠償請求権の成否(争点8)
原告は、
・TRK820のアトピー性皮膚炎患者の掻痒症の適用については、平成17年3月に マルホ株式会社 との間で共同開発及び販売権について契約を締結。
・肝用途の軟カプセル製剤「ノピコール」については、 東レ・メディカル に共同開発及び販売権について許諾。
・原告製剤(透析用途及び肝用途)について、・・・・・・鳥居薬品は独占的通常実施権を取得した上、同様に、特許権者である原告が製造した原告製剤の独占的な供給を受け、販売。
・鳥居薬品が先発医薬品である原告製剤の販売者であることは公にされており、鳥居薬品以外の販売者は市場に存在しなかった。
✔裁判所の判断
特許権者の許諾により設定される通常実施権は、特許権者との債権的な関係にすぎず、法律上、通常実施権者は、特許権者や専用実施権者のように特許発明を実施する権利を専有しているわけではない。しかし、民法709条の不法行為は、「法律上保護される利益」が侵害された場合に成立するのであり、被侵害利益が法律上排他性のある権利であることまでは要求されていない。本件においても、具体的事実関係に照らし、原告製剤の販売に関する鳥居薬品の利益が、その侵害者に対する関係で、不法行為法の観点から、法律上保護される利益であると認められるときは、鳥居薬品には、当該利益を違法に侵害されたことを理由とする固有の損害賠償請求権が認められるというべきである。
イ 単位数量当たりの利益の額(争点9)省略
ウ 販売することができないとする事情の有無及び当該事情に相当する数量等(争点10)
・代替品等に関する事情
✔裁判所の判断
止痒剤には多様なものが存するものの、ナルフラフィン製剤は、中枢神経系に作用することを特徴とし、既存治療で効果不十分な場合に投与されるから、他の種類の止痒剤とは市場を異にするものと認められ、ナルフラフィン製剤と他の種類の止痒剤とが同一市場で競合することはない。・・・・・・OD錠は、服用に水を必要としないという利便性があり、当該利便性は、ナルフラフィンの服用を要する患者の特徴(嚥下能力が低下している高齢者、取水制限等がある患者)に沿うものであることが認められるから、カプセルがOD錠に代替し得るということはできず、ナルフラフィン製剤のOD錠はカプセルとは市場を異にすると考えられる。結局、ナルフラフィン製剤OD錠である原告製剤について、被告製剤以外の競合品や代替品は見当たらないのであり、現に前記のとおり、ナルフラフィン製剤OD錠の市場では、原告製剤の消化数量の減少と被告製剤の販売数量の増加については、統計的相関関係が認められることが指摘されている。
・後発医薬品の普及促進等に関する事情と価格差に関する事情
✔裁判所の判断
・・・・・・ナルフラフィン製剤を服用する慢性腎疾患・肝疾患の患者は、高額療養費制度等において長期高額疾病患者の負担軽減措置等を受けることが見込まれ、このような場合には、患者の医療保険の自己負担額が多額にならないことから、患者において後発品を選ぶインセンティブが働かず、先発医薬品から後発医薬品への置き換わりが進まない場合があることが指摘されている。そうすると、一般的に後発医薬品の普及促進策が推進されているからといって、本件において当該後発医薬品の普及促進策の存在や原告製剤と被告製剤との形式的な価格差を理由に、侵害行為がなかった場合に、原告が被告製剤と同じ数量を販売することができなかったはずであるとはにわかに認めることはできず、他にこれを認めるに足りる的確な証拠はない。
・被告らのブランド力等に関する事情
✔裁判所の判断
被告らの営業努力やブランド力の存在を指摘し、被告らには後発医薬品会社として一定の知名度や好感度があることは認められるが、・・・・・・OD錠がナルフラフィン製剤の服用を要する多くの慢性腎疾患・肝疾患の患者の特徴に沿う剤形の薬剤であることを前提とすると、被告製剤が市場に存在しなければ原告製剤が購入されていた蓋然性が高く、・・・・・・被告らの主張する営業努力やブランド力は一般論を述べたものにすぎず、本件において、「販売することができないとする事情」になると認めることはできない。
以上によれば、原告について特許102条1項1号の「販売することができないとする事情」を認めることはできない。
解説/検討
審査の過程で、文言上、塩を除いてしまってはいたが、通常フリー体と塩の薬効が大きく異なることはないし、実際に原告製品でも塩酸塩が用いられているのだから、この補正のみによって権利範囲に属さないと判断されるのは酷であり、妥当な判決だろうと思う。「有効成分」を、技術常識に基づき権利範囲に包含されると解釈できたことで、先発メーカーが保護される実情に即した判決となったといえると思う。
<参考資料>