【添加剤の差異が存在する場合に添加剤の付加ないし転換が周知・慣用技術に基づくものと認めるに足りる証拠はないとして医薬品として実質同一なものではないと判断した事例】
投稿日:2026年5月12日 |

著者:弁護士 亀山 和輝
|
参照条文/キーワード/論点 |
特許法68条の2/医薬品として実質同一なもの |
ポイント
※本件は、有効成分ではない「成分」に関し、添加剤に相違がある原告製品に対し、被告の有する特許権の延長登録の効力が及ぶかが問題となった事例である。 |
判決概要 |
| 裁判所 | 東京地方裁判所民事第47部 |
| 判決言渡日 | 令和7年5月15日 |
| 事件番号 | 令和5年(ワ)第70527号、 令和6年(ワ)第70016号 |
| 事件名 | 消極的確認請求事件 損害賠償請求反訴事件 |
| 裁判長裁判官
裁判官 裁判官 |
杉浦 正樹
石井 奈沙 志摩 祐介 |
事案の概要
第1 事案の概要
本件本訴は、「販売名:ダサニチブ錠20mg サワイ効能・効果:1 慢性骨髄性白血病、2 再発又は難治性のフィラデルフィア染色体陽性急性リンパ性白血病」等の各製剤(以下、これらを併せて「原告製品」という。)を製造販売する原告が、発明の名称を「環状タンパク質チロシンキナーゼ阻害剤」とする発明に係る特許第3989175号(以下「本件特許」といい、その特許権を「本件特許権」という。)の特許権者である被告に対し、存続期間の延長登録を受けた本件特許権の効力は、原告による原告製品の生産、譲渡及び譲渡の申出に及ばない旨を主張して、主位的にはその旨の確認を求めると共に、予備的に、被告が原告に対して本件特許権に基づく差止請求権及び本件特許権侵害の不法行為に基づく損害賠償請求権をいずれも有しないことの確認を求める事案である。
本件反訴は、被告が、原告製品は本件特許に係る発明のうち特許請求の範囲請求項9記載の発明(以下「本件発明」という。)の技術的範囲に属し、延長後の本件特許権の効力は原告による原告製品の生産等に及ぶ旨を主張して、原告に対し、本件特許権侵害の不法行為に基づき、損害賠償および遅延損害金の支払を求める事案である。
第2 本件特許権及びその延長登録
1 本件特許権
特許番号 特許第3989175号
登録日 平成19年7月27日
出願番号 特願2000-611914号
出願日 平成12年4月12日
優先日 平成11年4月15日(優先権主張国 アメリカ合衆国)
発明の名称 環状タンパク質チロシンキナーゼ阻害剤
特許請求の範囲(請求項9)
「下式
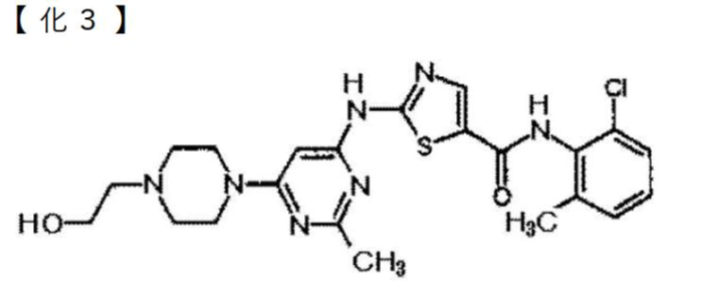
の化合物またはその塩。」
2 本件特許権の延長登録
被告は、本件特許権につき存続期間の延長登録出願をし、その登録を受けた。
争点
第3 争点(反訴請求について)
(1)延長登録された本件特許権の効力と原告製品(争点1)
(2)本件各延長登録の無効理由の有無(争点2)
ア 本件各処分によって禁止が解除された行為が本件発明の実施に該当する行為に含まれないこと(争点2-1)
イ 延長期間が過分であること(争点2-2)
(3)被告の損害(争点 3)
以下では、争点1についてのみ取り上げる。
判旨
(規範部分)
(1)延長された特許権の効力の及ぶ範囲について
ア 特許法68条の2は、特許権の存続期間の延長登録の制度趣旨が、政令処分を受けることが必要であったために特許発明の実施をすることができなかった期間を回復することを目的とするものであることに鑑み、存続期間が延長された場合の当該特許権の効力について、その特許発明の全範囲に及ぶのではなく、「政令で定める処分の対象となつた物(その処分においてその物の使用される特定の用途が定められている場合にあつては、当該用途に使用されるその物)」についての「当該特許発明の実施」にのみ及ぶ旨を定めるものである。同条は、「政令で定める処分の対象となつた物」(「当該用途に使用されるその物」を含む。以下同じ。)の範囲内では、政令処分を受けることが必要であったために特許発明を実施することができなかった特許権者を救済するために、延長された特許権の効力を及ぼすことが必要と認められる反面、その範囲を超えて延長された特許権の効力を及ぼすことは、期間回復による不利益の解消という限度を超えて特許権者を有利に扱うことになり、前記の延長登録の制度趣旨に反するばかりか特許権者と第三者との衡平を欠く結果となることから、前記のとおり定められたものである。
イ 「政令で定める処分の対象となつた物」に係る特許発明の実施行為の範囲について
(ア)「政令で定める処分」が薬機法所定の医薬品に係る承認に係るものである場合、同承認に必要な審査の対象となる事項等に鑑みると、存続期間が延長された特許権は、具体的な政令処分で定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」についての「当該特許発明の実施」の範囲で効力が及ぶと解するのが相当である。
そうすると、相手方が製造等する製品(以下「対象製品」という。)につき、具体的な政令処分で定められた「成分、分量、用法、用量、効能及び効果」において異なる部分が存在する場合、対象製品は、存続期間が延長された特許権の効力の及ぶ範囲に属するということはできない。もっとも、政令処分で定められた上記審査事項を形式的に比較して全て一致しなければ特許権者による差止め等の権利行使を容易に免れることができるとすれば、延長登録制度の趣旨に反するのみならず、衡平の理念にもとる結果になる。このような観点から、存続期間が延長された特許権に係る特許発明の効力は、政令処分で定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」(医薬品)のみならず、これと医薬品として実質同一なものにも及ぶというべきであり、第三者はこれを予期すべきである。
したがって、政令処分で定められた上記構成中に対象製品と異なる部分が存する場合であっても、当該部分が僅かな差異又は全体的にみて形式的な差異に過ぎないときは、対象製品は、医薬品として政令処分の対象となった物と実質同一なものに含まれ、存続期間が延長された特許権の効力の及ぶ範囲に属するものと解される。
(イ)ここで、医薬品の成分を対象とする物の特許発明において、政令処分で定められた「成分」に関する差異、「分量」の数量的差異又は「用法、用量」の数量的差異のいずれか1つないし複数があり、他の差異が存在しない場合に限定してみれば、僅かな差異又は全体的にみて形式的な差異かどうかは、特許発明の内容(当該特許発明が、医薬品の有効成分のみを特徴とする発明であるか、医薬品の有効成分の存在を前提として、その安定性ないし剤型等に関する発明であるか、又は、その技術的特徴及び作用効果はどのような内容であるかなどを含む。以下同じ。)に基づき、その内容との関連で、政令処分において定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」と対象製品との技術的特徴及び作用効果の同一性を比較検討して、当業者の技術的常識を踏まえて判断すべきである。
上記場合において、対象製品が政令処分で定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」と医薬品として実質同一なものに含まれる類型の1つとして、「医薬品の有効成分のみを特徴とする特許発明に関する延長登録された特許発明において、有効成分ではない「成分」に関し、対象製品が、政令処分申請時における周知・慣用技術に基づき、一部において異なる成分を付加、転換等しているような場合」を挙げることができる。この場合、その差異は上記「僅かな差異又は全体的にみて形式的な差異」に当たり、対象製品は、医薬品として政令処分の対象となった物と実質同一なものに含まれるというべきである(以上、本判決「第4の1」)。
(事実認定)
ウ 原告製品とスプリセル錠の成分等
スプリセル錠と原告製品の各添付文書における有効成分や添加剤に係る記載を項目ごとに対比すると、以下のとおりである(下線部は相違する点を示す。なお、添加剤のうち「乳糖水和物」及び「乳糖」が同じ物質であることは、当事者間に争いがない。)。

…(略)…
カ 原告の行った各種試験等について
(ア)ダサチニブ無水物原薬と添加剤の接触試験
原告が平成29年1月~同年3月を試験期間として実施したダサチニブ無水物の原薬と添加剤の接触による純度の変化を測定する試験に係る令和6年8月6日付け「試験結果報告書(接触試験)」(甲25)には、要旨、以下の記載がある。
…(略)…
(イ)ダサチニブ水和物/無水物の原薬の光安定性試験
原告が実施したダサチニブ水和物とダサチニブ無水物の原薬の光安定性に関する試験に係る令和6年6月5日付け「試験結果報告書(原薬光安定性)」(甲17)には、以下の記載がある。
…(略)…
(ウ)ダサチニブ水和物及びダサチニブ無水物の平衡溶解度ないし溶出性について
a 平衡溶解度について
…(略)…
b 溶出率について
…(略)…
(エ)生物学的同等性試験の非同等リスクに関する試験
原告が原告製品開発時に行った実験結果に係る令和6年11月12日付け「試験結果報告書(生物学的同等性試験の非同等リスクについての評価)」(甲30)は、ヒトの消化管内におけるpH変動を想定したpHシフト試験により評価した結果を報告するものであるところ、同報告書には、以下の記載がある。
…(略)…
(オ)添加剤グレードの試験
原告が原告製品の開発時に行った実験結果に係る令和6年11月12日付け「試験結果報告書(添加剤グレードの検討)」(甲31)は、pH1.2における溶出挙動を先発製剤に近づけるために行った添加剤グレードの検討について報告するものであるところ、同報告書には以下の記載がある。
…(略)…(以上、本判決「第4の1⑵」内参照)
(3)検討
ア …(略)…本件発明は、専ら医薬品の有効成分となる新規化合物を対象とした発明であり、医薬品の有効成分のみを特徴とする特許発明と理解される。
前記のとおり、医薬品の有効成分のみを特徴とする特許発明に関する延長登録された特許発明において、有効成分ではない「成分」に関し、対象製品が、政令処分申請時における周知・慣用技術に基づき、一部において異なる成分を付加、転換等しているような場合、対象製品は、医薬品として政令処分の対象となった物と実質同一なものに含まれると解すべきである。
本件における「対象製品」たる原告製品は、政令処分で定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」であるスプリセル錠との比較において、有効成分ではない「成分」に関し、スプリセル錠が添加剤としてPEG400を添加するのに対し、原告製品ではこれを添加しておらず、コーティング剤としてカルナウバロウが添加されている。このような差異について、ダサチニブ水和物を有効成分とするスプリセル錠は、安定性試験でコーティング剤中に生じた分解物の生成を抑えるためにPEGを添加したものとみられる。他方、原告製品は、吸湿性や安定性においてダサチニブ水和物に劣るダサチニブ無水物を有効成分とするところ、安定性につき、PEGを含む場合よりもHPCを混合した方が優れることを確認し、PEGをHPCに転換したものとみられる。これに加え、原告は、ダサチニブ無水物はダサチニブ水和物に比して平衡溶解度ないし溶出性が高い性質を有すると考えられるところ、結晶セルロース及びHPCのグレードを検討した結果を踏まえ、スプリセル錠に溶出挙動が近いものを選択したとみられる。さらに、安定性においてダサチニブ無水物がダサチニブ水和物に劣る点については、証拠(甲18、29)及び弁論の全趣旨によれば、原告製品の酸化チタンの含有量を20%とし、コーティング剤の厚みを20mg 錠については素錠の4.0%w/w、50mg錠については3.5%w/wとすると共に、光安定性を高めるために多量の酸化チタンが含まれることなどを原因として錠剤の滑り性が劣ることから、スプリセル錠に含まれない成分であるカルナウバロウを添加したとみられる。
以上のとおり、本件における「対象製品」たる原告製品は、政令処分で定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」であるスプリセル錠と対比すると、有効成分ではない「成分」であるPEGを転換すると共に、カルナウバロウを添加しており、スプリセル錠(ダサチニブ水和物)と原告製品(ダサチニブ無水物)との有効成分の違い等に起因する課題を踏まえ、上記添加剤の付加ないし転換を行っているものとみられる。このような添加剤の付加ないし転換が周知・慣用技術に基づくものと認めるに足りる的確な証拠はなく、むしろ、原告が自己の技術等に基づき、原告製品の溶出挙動をスプリセル錠のそれに近付け、又はスプリセル錠との生物学的同等性を得るために、これらの添加剤の付加ないし転換を行ったことがうかがわれる。
したがって、原告製品は、医薬品としてスプリセル錠と実質同一なものに含まれるということはできない。
イ 被告の主張について
(ア)まず、被告は、原告製品は、後発医薬品として、先発医薬品と有効成分等が同一であることを前提に臨床試験が免除され、生物学的同等性試験のみを経ることで、先発医薬品と同等の品質、有効性及び安全性を備えるものとして製造販売の承認を受けているのであるから、原告製品とスプリセル錠とで差異があるとしても有意な差異とはいえない旨主張する。しかし、このような被告の主張は、要するに、医薬品の承認制度の面から、後発医薬品として承認されたものは全て実質同一物に当たるというに等しく、特許法68条の2の制度趣旨等に鑑みると直ちには採用できない。
(イ)また、被告は、本件発明はチロシンキナーゼ阻害作用を有するダサチニブという新規化合物に係る物質特許発明であり、「医薬品の有効成分のみを特徴とする発明」に当たるところ、「医薬品の有効成分」とは、上位概念としての化合物を意味するものであり、特定の存在形態に限定されない旨、及び、原告製品は、患者の体内でダサチニブがチロシンキナーゼ阻害作用を同程度に発揮する点で、スプリセル錠と同程度に本件発明の本質を備えており、その差異は僅かな差異又は全体的にみて形式的な差異に過ぎない旨を主張する。
確かに、本件明細書には、「本発明の化合物のプロドラッグや溶媒和物も本発明に含まれる。…好ましくは、式Iの化合物の溶媒和物は水和物である」(【0043】)との記載があることなどに鑑みると、ダサチニブ水和物とダサチニブ無水物というスプリセル錠と原告製品の有効成分における差異は、医薬品としての効能に影響しないことがうかがわれる。しかし、政令処分が薬機法所定の医薬品に係る承認である場合、当該政令処分を受けることが必要であったために実施することができなかった物を特定するための事項としての「成分」は、有効成分に限られない。また、本件明細書には、生物活性に関する具体的なデータは開示されていないし、本件発明の化合物が有用とされる具体的な障害の処置の例として、スプリセル錠及び原告製品の効能・効果である「慢性骨髄性白血病」及び「再発又は難治性のフィラデルフィア染色体陽性急性リンパ性白血病」は明示的には示されておらず、加えて、医薬品を構成する添加成分等については一般的な例が開示されているにとどまり、具体的な医薬品の構成は開示されていない。これらの事情に鑑みると、本件発明に係る特許の内容を踏まえても、ダサチニブ水和物とダサチニブ無水物という差異が医薬としての効能に影響しないことをもって、スプリセル錠と原告製品とが実質同一なものとみることは必ずしもできない。
(ウ)被告は、スプリセル錠と原告製品の違いは、前者にはPEGが含まれるのに対し、後者にはカルナウバロウが含まれている点だけであり、その余の添加剤は共通するところ、これらはいずれも周知慣用の医薬品添加剤である旨主張する。
このような添加剤の付加ないし転換が周知・慣用技術に基づくものと認めるに足りる的確な証拠はないことは前記のとおりである。また、これらの添加剤それ自体が周知慣用の成分であるとしても、当該添加剤の添加量や、その有効成分及び他の添加剤との関係のほか、具体的な製造に当たりいかなる添加剤を採用し、どのように添加をするかは、医薬品の性状・性質、更には医薬製剤としての作用効果に影響を与え得る。前記のとおり、原告は、自己の技術等に基づき、原告製品の溶出挙動をスプリセル錠のそれに近付け、又はスプリセル錠との生物学的同等性を得るために、これらの添加剤の付加ないし転換を行ったことがうかがわれることを踏まえると、添加されている添加剤の成分が周知慣用のものであることをもって直ちに原告製品とスプリセル錠の差異が僅かな差異又は全体的にみて形式的な差異に当たるとはいえない。
解説/検討
第六十七条第四項の規定により同条第一項に規定する存続期間が延長された場合…(略)…の当該特許権の効力は、その延長登録の理由となつた第六十七条第四項の政令で定める処分の対象となつた物…(略)…についての当該特許発明の実施以外の行為には、及ばない。
本判決は、スプリセル錠(ダサチニブ水和物)と原告製品(ダサチニブ無水物)との有効成分の違い等に起因する課題を踏まえ、原告が複数の試験を実施し、添加剤の付加ないし転換を行ったことがうかがわれることに着目した判断を行ったものと考えられる。
なお、延長登録された特許権の効力範囲(特許法68条の2)に関しては、本判決以後も、知財高判令和7年5月27日〔令和3年(ネ)第10037号〕(裁判所HPへのリンク)、大阪地判令和8年3月3日〔令和7年(ワ)第10786号、同第10790号〕(裁判所HPへのリンク)が出されている(当該判決に関する当職の拙解説へのリンク(当所HP))。